科研進(jìn)展
蘭州化物所氯代芳烴不對(duì)稱碳?xì)滢D(zhuǎn)化獲進(jìn)展
氯代芳烴是有機(jī)合成中最常用的化合物,發(fā)展該類(lèi)分子的區(qū)域和對(duì)映選擇性碳?xì)滏I活化能為手性芳烴分子的合成提供直接且具有吸引力的方法。然而,由于氯代芳烴與金屬極弱的結(jié)合力,這一過(guò)程面臨著活性低和區(qū)域選擇性控制難的問(wèn)題。
中國(guó)科學(xué)院蘭州化學(xué)物理研究所羰基合成與選擇氧化國(guó)家重點(diǎn)實(shí)驗(yàn)室徐森苗團(tuán)隊(duì)(有機(jī)硼催化組)一直致力于過(guò)渡金屬催化的區(qū)域和立體選擇性碳?xì)滏I硼化反應(yīng)。他們通過(guò)發(fā)展新策略,實(shí)現(xiàn)了烯烴的區(qū)域和立體選擇性硼氫化反應(yīng);發(fā)展了一類(lèi)以 1,2-二苯基乙二胺為手性骨架、具有強(qiáng) 給電子能力的新型手性雙齒硼基配體( CBL),能在溫和條件下加速過(guò)渡金屬銥對(duì)惰性 C-H鍵的化學(xué)、區(qū)域和立體選擇性氧化加成,實(shí)現(xiàn)了一系列不對(duì)稱 C-H鍵硼化新反應(yīng),為中心手性、平面手性和軸手性的快速構(gòu)建提供了原子和步驟經(jīng)濟(jì)的方法。
近日,該團(tuán)隊(duì)針對(duì)氯代芳烴配位能力弱、反應(yīng)活性低、區(qū)域選擇性控制難的問(wèn)題,利用手性 CBL的邊臂效應(yīng),成功實(shí)現(xiàn)了氯代芳烴類(lèi)化合物的高區(qū)域和對(duì)映選擇性碳?xì)滏I硼化反應(yīng),最高對(duì)映選擇性可大 于99%(圖 1),獲得了高達(dá) 7000的催化轉(zhuǎn)化數(shù),這是目前官能團(tuán)導(dǎo)向的過(guò)渡金屬催化不對(duì)稱碳?xì)滏I活化領(lǐng)域的最高值。產(chǎn)物中的 C-B、 C-H和 C-Cl鍵均可方便地轉(zhuǎn)化成其它官能團(tuán),豐富了手性聯(lián)苯的化學(xué)空間。
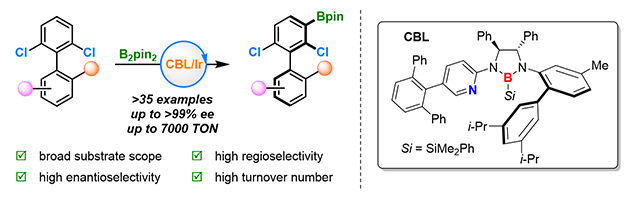
圖 1. CBL/Ir催化氯代芳烴的區(qū)域和對(duì)映選擇性 C-H鍵硼化反應(yīng)
相關(guān)成果以“ Aryl Chloride-Directed Enantioselective C( sp2) -H Borylation Enabled by Iridium Catalysis” 為題發(fā)表在 J. Am. Chem. Soc. (論文鏈接: https://pubs.acs.org/doi/10.1021/jacs.3c08129)上。
以上工作得到了科技部、國(guó)家自然科學(xué)基金委、蘭州化物所和杭州師范大學(xué)開(kāi)放基金的支持。
發(fā)表文章列表:








